Neue Klassifikation soll für mehr Klarheit sorgen
Bericht: Regina Scharf, MPH, Redaktorin
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die Glomerulonephritis ist eine komplizierte Angelegenheit. Das liegt auch daran, dass die immunvermittelten Erkrankungen anhand von histopathologischen Mustern beschrieben werden, die keinen Rückschluss auf die Ursache und Therapie zulassen. Eine neu vorgeschlagene Klassifikation soll das nun ändern.
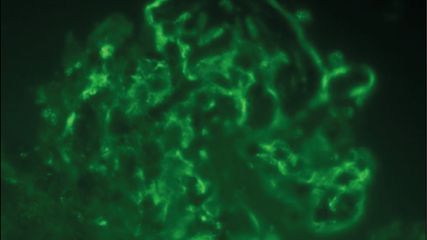
Die Glomerulonephritis (GN) ist ein Überbegriff für relativ seltene immunvermittelte Erkrankungen, die zu einer Schädigung der Glomeruli, einer chronischen Nierenerkrankung und einem irreversiblen Verlust der Nierenfunktion führen. Die klinischen Zeichen sind mit arterieller Hypertonie, Proteinurie und Hämaturie relativ unspezifisch. Die Diagnose wird bestätigt durch eine Nierenbiopsie. Die Kategorisierung der GN in Subgruppen basiert auf der Beschreibung der histopathologischen Läsionen, beispielsweise mesangio- oder membranoproliferative GN, membranöse GN etc., und hat historische Gründe – namentlich die Einführung der Nierenbiopsie und die Untersuchung unter dem Lichtmikroskop.1,2
Mit dem heutigen Wissen, den verfügbaren diagnostischen und therapeutischen Methoden scheint das Vorgehen überholt. «Was wir unter dem Mikroskop sehen, sind immer die gleiche Entzündung und Fibrose», sagte Prof. Dr. med. Hans-Joachim Anders von der Ludwig-Maximilians-Universität in München am Jahreskongress der Schweizerischen Gesellschaft für Nephrologie. Dabei handle es sich lediglich um die Folgen der Erkrankung. Die aktuelle Nomenklatur und Klassifikation liefern jedoch keine Antwort auf die Pathogenese. Das sei vertretbar gewesen, solange man keine andere Therapie als Glukokortikoide zur Verfügung gehabt hätte. «Der häufigste Grund für eine Nierenbiopsie war, dass man wissen wollte, ob es eine Indikation für Steroide gibt oder nicht», sagte der Spezialist. In der Zwischenzeit haben sich die Dinge geändert: Mittels Methoden wie Immunphänotypisierung und Gendiagnostik wurde gezeigt, dass vergleichbare histologische Läsionen durch unterschiedliche Erkrankungen verursacht werden können, die eine komplett andere Behandlung erfordern.1 Zudem steht heute eine Vielzahl von spezifisch wirksamen Medikamenten für die Behandlung der verschiedenen Entitäten der GN zur Verfügung.
GN-AC-Einteilung
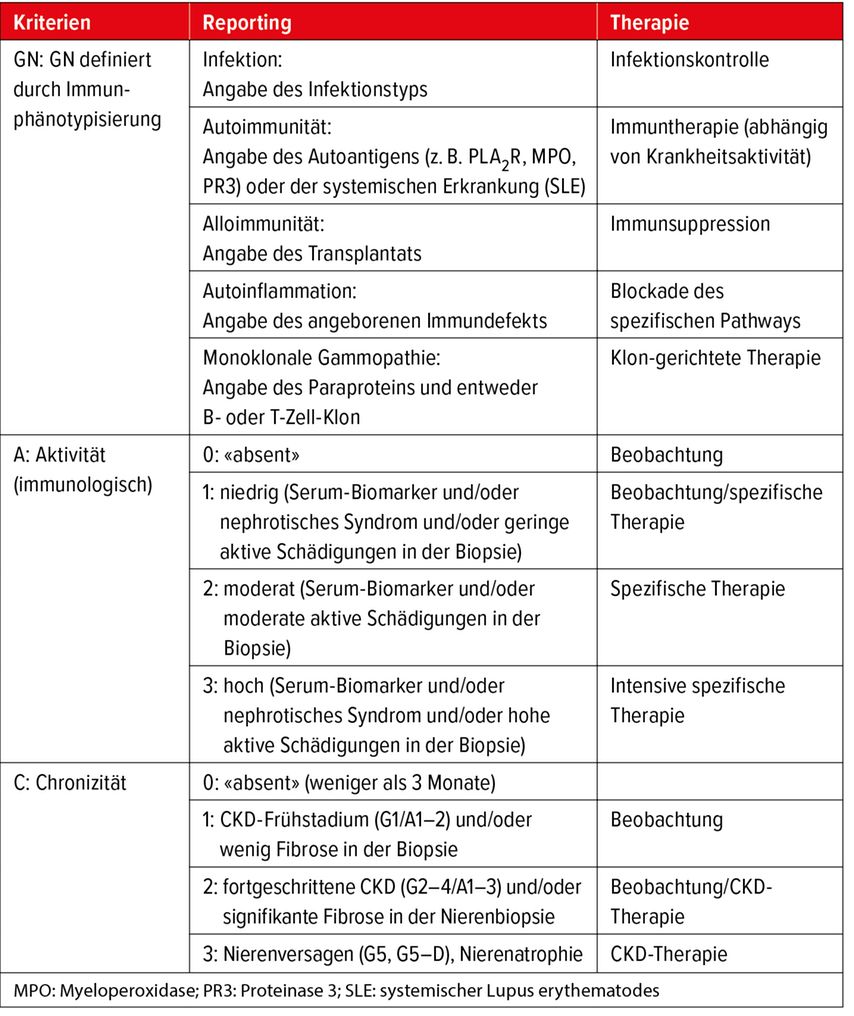
Anders schlug eine einfache Klassifikation vor, die direkt mit der Immuntherapie verlinkt ist (Tab.1).1 Entsprechend den wichtigsten zugrunde liegenden Immunmechanismen lässt sich die GN in 5 Kategorien einteilen.
Tab. 1: Vorgeschlagene GN-AC-Klassifikation inkl. der Berichterstattung bei Glomerulonephritis (adaptiert nach Romagnani P et al.)1
Infektionsbedingte GN
Dabei handelt es sich weltweit um die häufigste Form der GN. Auslöser sind Hepatitisviren, Bakterien wie Streptokokken und Staphylokokken sowie Parasiten wie Plasmodien und Schistosomen. Die GN tritt als Folge einer Abwehrreaktion gegen eine akute, subakute oder persistierende Infektion auf. Immunologisch gesehen existieren drei Hauptmechanismen.1 «Bei einer persistierenden Infektion sollte immer auch an einen primären oder sekundären Immundefekt gedacht werden», so Anders. Dies sei auch in Hinblick auf eine immunsuppressive Therapie wichtig.
Für die Therapie der infektionsbedingten GN muss der Krankheitserreger identifiziert werden. «Gelingt uns das, können wir die Erkrankung erfolgreich behandeln», sagte Anders und verwies auf die positiven Erfahrungen bei Patienten mit Hepatitis C und HIV.
Monoklonale Gammopathie-bedingte GN
Diese Form der Glomerulonephritis ist insgesamt selten. «Bei Personen über 50 Jahre mit Glomerulonephritis sollte man allerdings immer nach einer monoklonalen Gammopathie suchen, denn in diesem Alter ist sie eine häufige Ursache.»
Der Auslöser ist ein B-Zell- oder Plasma-Zell-Klon im Knochenmark, der nephrotoxische Immunglobuline oder Immunglobulinkomponenten produziert. Die Behandlung dieser sogenannten «monoclonal gammopathies of renal significance» (MGRS) besteht in einer klongerichteten Therapie und orientiert sich am Behandlungsalgorithmus des multiplen Myeloms.1
Autoinflammatorisch bedingte GN
Die autoinflammatorische GN ist die Folge einer angeborenen Fehlfunktion des Immunsystems, die zu einer erhöhten Zytokinaktivität, beispielsweise von Interleukin (IL) 1, Tumornekrosefaktor (TNF) α oder Typ-1-Interferon, führt. Diese können zu Entzündungsreaktionen mit Organschäden führen, beispielsweise zu einer Lupusnephritis. In diese Gruppe gehören auch die komplementvermittelten Erkrankungen wie zum Beispiel die C3-Glomerulonephritis (C3GN).1 Die Diagnose wird anhand eines genetischen Tests gestellt. Die Behandlung besteht in einer gezielten Immuntherapie: «Keine Steroide oder Mycophenolat-Mofetil, sondern eine selektive Blockade des dysregulierten Pathways und die Erkrankung ist unter Kontrolle», sagte Anders.
Autoimmunbedingte GN
Diese Form der GN tritt als Folge einer adaptiven Immunantwort auf eine oder mehrere Autoantigene auf. Die Autoimmunität ist die Folge eines Toleranzverlusts, zu dem genetische und umweltbedingte Faktoren beitragen. Sobald die Toleranz verloren gegangen ist, entwickelt sich eine zelluläre oder humorale Autoimmunität. Diese kann vorübergehend auftreten oder zur Ausbildung von autoreaktiven T- und B-Gedächtniszellen und einem langfristigen Immungedächtnis führen. Eine erneute oder anhaltende Antigen-Exposition führt zu einer spezifischen immunologischen Aktivität, die sich in Form einer anhaltenden oder rezidivierenden Krankheitsaktivität manifestiert.1
Obwohl die klinische Präsentation variiert und die Muster der histologischen Läsionen sich je nach Lokalisation der Antigene unterscheiden, weisen die Mechanismen der zugrunde liegenden Immunreaktion Gemeinsamkeiten auf. «Viele Kollegen meinen, dass es sich bei IgA-GN, ANCA-assoziierter GN oder Lupusnephritis um unterschiedliche Erkrankungen handelt. Aus immunologischer Perspektive funktionieren sie aber genau gleich», sagte der Referent. Worin sie sich unterscheiden, sind die Antigene und die klinische Präsentation. Die Behandlung basiert auf Medikamenten, die auf einzelne Elemente des adaptiven Immunsystems abzielen, die bei der autoimmunen GN eine Rolle spielen, wie z.B. Azathioprin, MMF, Calcineurin-Inhibitoren, B-Zell-depletierende Wirkstoffe und Belimumab sowie Glukokortikoide.
Alloimmunitätsbedingte GN
Die adaptive Immunreaktion bei dieser GN-Form weist Ähnlichkeiten mit der oben beschriebenen autoimmunitätsbedingten GN auf. Sie tritt bei Personen nach einer allogenen Transplantation von Organen, Knochenmark oder Zellen auf. Die Immunität richtet sich gegen HLA- und Nicht-HLA-Antigene.1 Zur Therapie der Alloimmunität im Allgemeinen und bei alloimmunitätsbedinger GN werden aktuell die gleichen Medikamente eingesetzt wie zur Kontrolle bei Autoimmunität.
Bestimmung der Krankheitsaktivität
Die Kategorisierung der GN anhand ihrer Pathogenese erfordert eine gründliche Immunphänotypisierung mittels genetischer Tests, mikrobiologischer und serologischer Untersuchungen, erweiterter Suche nach Autoantikörpern, Komplementuntersuchungen im Serum, Knochenmarkspunktion usw.1 Die Nierenbiopsie bleibt auch in Zukunft ein wichtiges diagnostisches Instrument: «Sie bestätigt, ob eine GN vorliegt oder nicht, und liefert dort, wo spezifische Serum-Biomarker fehlen, verlässliche Informationen über die Krankheitsaktivität und Chronizität», so Anders. Letzteres ist entscheidend für die Intensität der Immuntherapie und der Behandlung der chronischen Nierenerkrankung (CKD). Für beide Indikationen stehen heute mehrere Therapieoptionen zur Verfügung.
Der Spezialist riet davon ab, die Höhe der Proteinurie zur Einschätzung der Krankheitsaktivität bei einer GN heranzuziehen. Diese sei ein schlechter Biomarker. Typische Gründe für eine Proteinurie bei Personen mit einer inaktiven GN sind zum Beispiel Adipositas, hohe Salz- oder Proteinzufuhr, eine reduzierte Anzahl an Nephronen, glomeruläre Schäden, Diabetes mellitus und eine Therapie mit Vasodilatanzien. Alle diese Faktoren müssen immer erst kontrolliert werden, bevor man eine Proteinurie als Marker für die immunologische Aktivität interpretiert.
Quelle:
Jahreskongress der Schweizerischen Gesellschaft für Nephrologie (SGN/SSN), 5.–6. Dezember 2024, Basel
Literatur:
1 Romagnani P et al.: Nephrol Dial Transplant 2023; 38: ii3-10 2 Anders HJ et al.: Nat Rev Immunol 2023; 23: 453-71
Das könnte Sie auch interessieren:
Was wir wirklich wissen und wo der Mythos beginnt
Dass eine chronische Niereninsuffizienz mit dem Vorliegen einer metabolischen Azidose einhergeht, ist längst bekannt. Aber bedingt sie auch ihre Progression? Und kann den Betroffenen mit ...
Prävention von Nierensteinen mit Thiaziden: top oder Flop?
Trotz unklarer Datenlage werden Thiazide und Thiazid-ähnliche Diuretika seit Jahrzehnten zur Prävention von idiopathischen Nierensteinen eingesetzt. Die NOSTONE-Studie, eine vom ...
Lupusnephritis: frühzeitig erkennen – richtig behandeln
Die Lupusnephritis ist eine der wichtigsten Organmanifestationen des systemischen Lupus erythematodes, da sie entscheidend zur Morbidität und Mortalität der Erkrankung beiträgt. Die ...